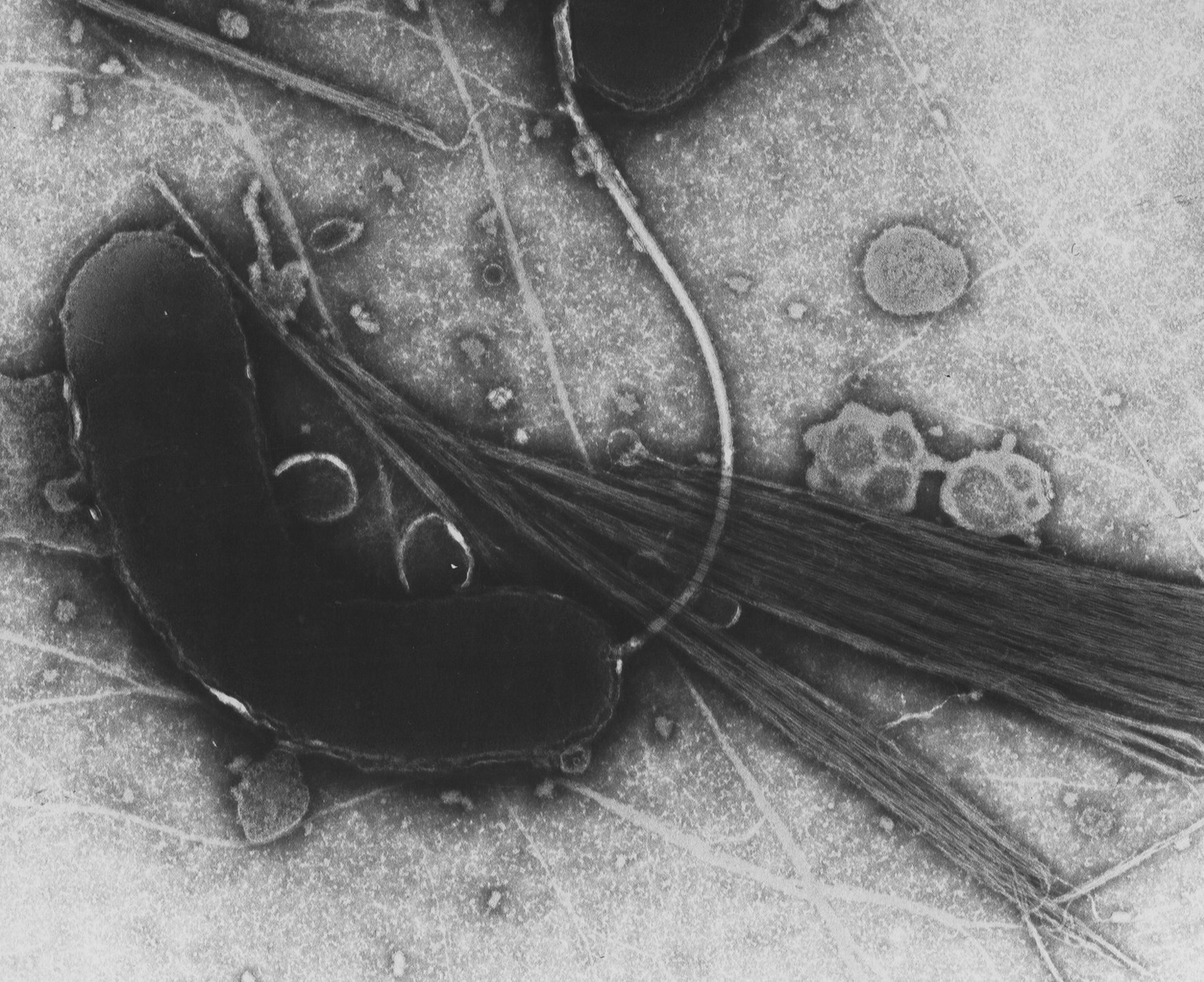
Eine Studie zum Cholera-Bakterium lieferte einen neuen Therapieansatz, der für fast alle Infektionserkrankungen anwendbar sein könnte. Neue Medikamente könnten Antibiotika ersetzen und damit das natürliche Mikrobiom im Darm verschonen.
Cholera ist eine schwere bakterielle Infektionskrankheit, die durch das Bakterium Vibrio Cholerae verursacht wird. Die Infektion erfolgt meist über verunreinigtes Trinkwasser oder infizierte Nahrung. Wird Cholera nicht behandelt, so liegt die Todesrate bei 20 bis 70 Prozent.
Das Cholera-Bakterium überlebt zwischen den Epidemien im Wasser und muss dort mit ganz anderen Bedingungen klar kommen, als im menschlichen Körper. Der Mechanismus, der für das Überleben des Cholera-Bakteriums in den vollkommen verschiedenen Umgebungen verantwortlich ist, war bisher unklar.
Cholera-Bakterien sind anpassungsfähig
Jetzt entdeckte der Doktorand Franz Zingl vom Institut für Molekulare Biowissenschaften, an der Universität Graz, dass die Outer Membrane Vesicles (OMVs) des Cholera-Bakteriums für diese außerordentliche Anpassungsfähigkeit verantwortlich sind. OMVs sind Ausstülpungen der Außenhaut, welche die Cholera-Bakterien durch Abschnüren abstoßen können. Dieser Prozess ist sehr energieaufwändig. Den Mikroorganismen hilft er, sich schneller an die für sie widrigen Bedingungen im Wirt anzupassen – und der Immunabwehr zu entgehen.
Umstellung der Ernährung
Die Außenhaut des Cholera-Bakteriums ist auch für dessen Ernährung verantwortlich und verfügt über zahlreiche Aufnahmesysteme von Nährstoffen – darunter auch das sogenannte Porin OmpT. Im menschlichen Körper würde dieses Gallensalze und antimikrobielle Peptide aufnehmen und das wäre für das Cholera-Bakterium tödlich.
Um dies zu verhindern, bildet das Bakterium kein neues Porin OmpT mehr. Wie die bereits vorhandenen Schleusen entfernt werden können, war bisher nicht bekannt.
Verstärkung der Barriere
Das Team um den Doktoranden konnte zeigen, dass die Krankheitserreger beim Eintritt in den Wirt massiv Außenhaut-Ausstülpungen abstoßen. Das ist der Mechanismus, mit dem das Cholera-Bakterium die nicht mehr benötigten Porine Ompts entsorgt. Gleichzeitig werden die sogenannten Lipopolysaccharide ( LPS) abgestoßen. Diese verfügen über keine ausreichende Barriere gegen die Immunabwehr des Körpers und werden durch neue LPS ersetzt. Fest aneinander gekettet, sind diese fähig, die Membran undurchlässiger zu machen.
Auslöser Eisenmangel
Der Mechanismus wird durch eine Abwehrreaktion des menschlichen Körpers ausgelöst: Das Cholera-Bakterium benötigt – wie auch der menschliche Körper – für alle biologischen Vorgänge das Spurenelement Eisen. Der menschliche Körper bindet das Eisen um es dem Eindringling zu verweigern. Der Eisenmangel verursacht beim Cholera-Bakterium Stress und es reagiert mit dem Abstoßen der OMV’s (Vesikulierung). Die Vesikulierung verschafft den Krankheitserregern einen klaren Wettbewerbsvorteil bei der Besiedlung des Wirts.
Auch Antibiotika könnten auslösend wirken
Darüber hinaus gibt es Indizien dafür, dass der Kontakt zu Antibiotika oder Desinfektionsmitteln in niedrigen Dosen ebenfalls ein Abschnüren der Außenmembran-Vesikel auslöst. Daraus schließt der Molekularbiologe, dass Rückstände von keimtötenden Medikamenten in Wasser oder Nahrung problematisch sind, weil sie den Cholera-Bakterien einen „Fitnessvorteil“ verschaffen können.
Neue Therapieansätze
Untersuchungen zu den Überlebensmechanismen des Cholera-Bakterium Vibrio cholerae sind für nahezu alle bakteriellen Krankheitserreger gültig – auch für Salmonellen, Pseudomonaden oder Neisserien.
Die Erkenntnisse sollen jetzt für neue Therapieansätze gegen Infektionserkrankungen genutzt werden: Die Forschenden suchen nach einer Substanz, welche die Vesikulierung hemmt. Damit könnte die körpereigene Immunabwehr leichter mit den Eindringlingen fertig werden. Die neuen Medikamente könnten Antibiotika ersetzen und damit das natürliche Mikrobiom im Darm verschonen.
Publikation:
Franz G. Zingl, Paul Kohl, Fatih Cakar, Deborah R. Leitner, Fabian Mitterer, Katherine E. Bonnington, Gerald N. Rechberger, Meta J. Kuehn, Ziqiang Guan, Joachim Reidl, Stefan Schild, „Outer Membrane Vesiculation Facilitates Surface Exchange and In Vivo Adaptation of Vibrio cholerae“, Cell Host & Microbe, DOI: 10.1016/j.chom.2019.12.002
Auch interessant:






