Das neuartige Coronavirus SARS-CoV-2 gibt den Wissenschaftlern weltweit noch zahlreiche Rätsel auf. Sicher ist nur, dass sich die Erreger nach einer Infektion in den menschlichen Zellen in rasender Geschwindigkeit vermehren. Das geschieht, indem das Virus sein Erbgut, das aus einem langen RNA-Strang besteht, mit einer viralen „Kopiermaschine“, der sogenannten Polymerase, vervielfältigt.
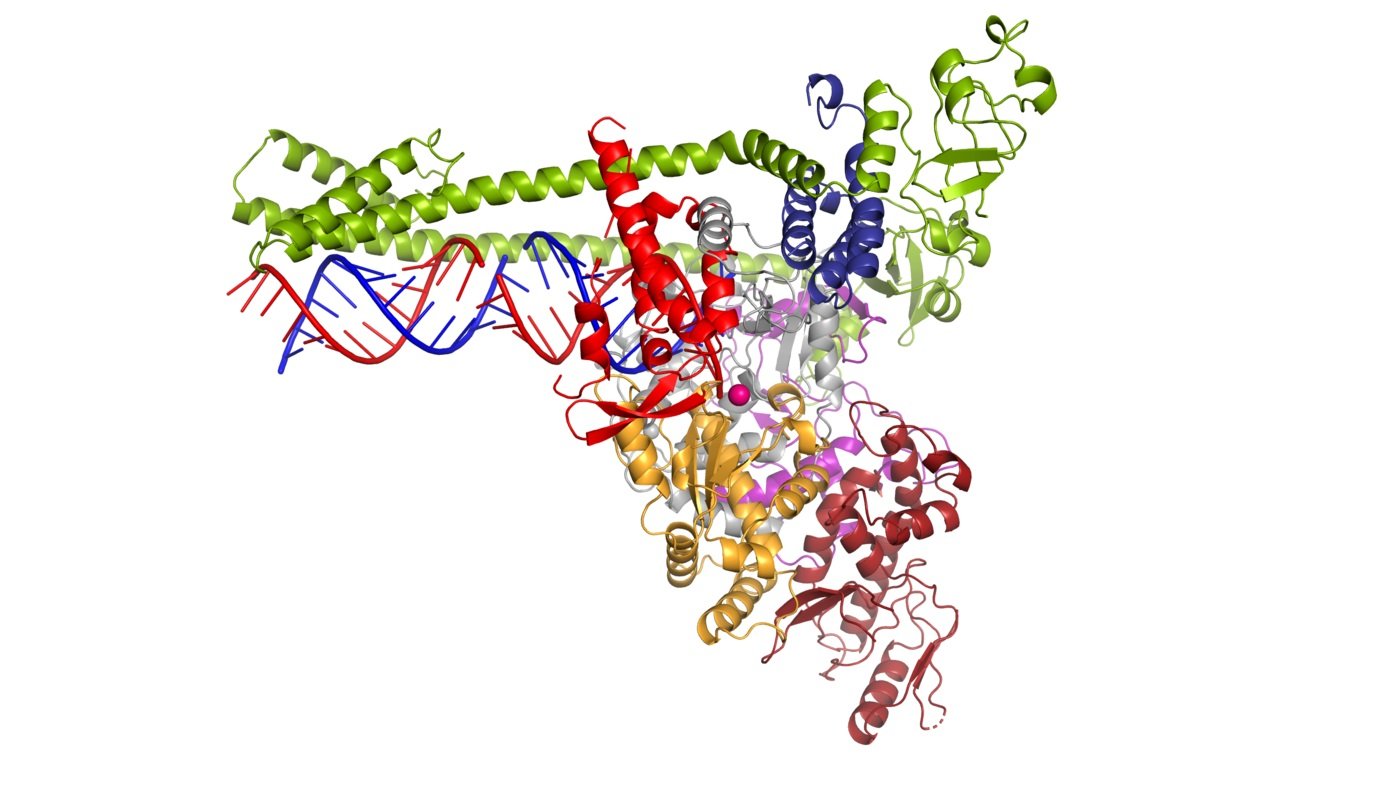
Forscher um Patrick Cramer vom Göttinger Max-Planck-Institut für biophysikalische Chemie sind nun einen großen Schritt in der Erforschung des Virus weitergekommen: Sie haben die räumliche Struktur der Corona-Polymerase entschlüsselt. Mit diesen Informationen könnten sie nun weiter erforschen, wie antivirale Substanzen – wie z.B. Remdesivir – wirken, die die Polymerase blockieren, erklären die Forscher. Darüber hinaus könnten aber auch neue Wirkstoffkandidaten gesucht werden.
„Im Angesicht der derzeitigen Pandemie wollten wir helfen“, sagt Max-Planck-Direktor Cramer. „Wir verfügen über umfassende Erfahrung, Polymerasen zu untersuchen.“ Das Überraschendste sei dabei gewesen, dass der Aufbau der Coronavirus-Kopiermaschine aus der Reihe falle, und sich von allen anderen Polymerase-Strukturen unterscheide, sagt Forschungsgruppen-Mitglied Hauke Hillen.
Zwar binde die Corona-Polymerase auf die gleiche Weise an die RNA, wie es auch anderen Virusarten tun, sie besitze jedoch „ein weiteres Element, mit der sie sich an der RNA festklammert, bis sie das Erbgut kopiert hat.” Das sei gerade für das Coronavirus wichtig, denn sein Erbgut bestehe aus rund 30.000 Bausteinen und sei damit besonders lang. “Das Kopieren eine echte Mammutaufgabe.“
Alte Substanzen optimieren, neue finden
Auf dem Wissen aufbauend, wie die Coronavirus-Polymerase Atom für Atom aufgebaut ist, wollen die Forscher nun genauer untersuchen, wie antivirale Substanzen die Vermehrung von Coronaviren blockieren. „Auf Remdesivir, das die Corona-Polymerase direkt blockiert, ruhen viele Hoffnungen“, betont Cramer. „Durch die Polymerase-Struktur könnte es möglich werden, bereits vorhandene Substanzen wie Remdesivir zu optimieren und ihre Wirkung zu verbessern. Doch wir wollen auch nach neuen Substanzen fahnden, die die Virus-Polymerase stoppen können.“
Der Weg bis hin zur dreidimensionalen Struktur der Corona-Polymerase sei aber steinig gewesen, gibt das Team zu. „Zunächst mussten wir die Polymerase aus drei gereinigten Proteinen im Reagenzglas nachbauen. Nach einigen Optimierungen war sie schließlich funktionsfähig“, erläutert Goran Kokic. „Nur so konnten wir untersuchen, wie sie arbeitet.“ Um die Aktivität der Polymerase bestimmen zu können, hatte der Wissenschaftler extra einen speziellen Test entwickelt.
Eine Untersuchung der Proben im Elektronenmikroskop bei über 100.000-facher Vergrößerung führte jedoch zunächst in eine Sackgasse. „Obwohl wir zehn Tage und Nächte rund um die Uhr Bilder aufgenommen hatten, konnten wir keine detaillierten Einblicke in die Struktur gewinnen“, erinnert sich Christian Dienemann, der Experte für Elektronenmikroskopie im Team.
„Seltsame“ Probe bringt Durchbruch
Allerdings habe eine Probe anders ausgesehen, „irgendwie seltsam“ Deshalb wollten die Forscher sie auch verwerfen. Glücklicherweise habe man das aber nicht getan, sagt der Datenverarbeitungsexperte der Gruppe, Dimitry Tegunov. „Ausgerechnet diese Probe hat uns die hochwertigen Daten geliefert, die wir unbedingt brauchten.“
Im nächsten Schritt wollen die Göttinger Forscher nun nach Punkten suchen, die das Virus angreifbar machen. „Wir haben auch die sogenannten Helferfaktoren im Visier, die die Virus-RNA so verändern, dass sie durch das menschliche Immunsystem nicht abgebaut werden kann“, so Cramer. „Und natürlich hoffen wir als Strukturbiologen, weitere Angriffspunkte im Virus zu finden, die mittelfristig neue Therapiestrategien eröffnen.“
Die Ergebnisse ihrer Forschung haben Cramer und sein Team bereits im Internet veröffentlicht, um sie „sofort mit der internationalen Forschungsgemeinschaft teilen, denn es muss jetzt, wo wir uns mitten in der Pandemie befinden, besonders schnell gehen.“
Titelbild: Die Polymerase des neuartigen Coronavirus SARS-CoV-2 vervielfältigt das Erbgut (blau und rot) des Erregers. © Lucas Farnung, Christian Dienemann, Hauke Hillen / Max-Planck-Institut für biophysikalische Chemie