Normalerweise schlägt das menschliche Herz rund 60 bis 80 Mal pro Minute, bei rund einer Million Menschen in Deutschland – mehr als 33 Millionen weltweit – steigt der Herzschlag mitunter aber plötzlich auf bis zu 150 Schläge an. Sie leiden unter Vorhofflimmern, der häufigsten behandlungsbedürftige Herzrhythmusstörung in Deutschland. Während das Vorhofflimmern an sich im Allgemeinen nicht unmittelbar lebensgefährlich ist, können Folgen wie Herzinsuffizienz, Herzinfarkt, Blutgerinnsel und Schlaganfälle zu schwerwiegenden Folgen oder auch zum Tod führen.
Eine typische Behandlung des Flimmerns ist eine kathetergestützte Verödung krankhafter elektrischer Erregungsherde im Herzmuskelgewebe, die sogenannte Ablation. Hier kommt es jedoch häu.gfig vor, dass die Patienten nach der Behandlung ein sogenanntes atypisches Vorhofflattern entwickeln.
Beim Vorhofflattern, verläuft die elektrische Erregung des Herzens – anders als beim Vorhofflimmern – koordiniert. Dabei veranlassen ungewöhnlich schnelle elektrische Erregungsmuster die Vorhöfe zu raschen Kontraktionen. Die Auswirkungen sind aber die gleichen wie beim Vorhofflimmern: Herzrasen, Atemnot und Schwäche und auch das Schlaganfallrisiko ist erhöht.
Realitätsnahe Computermodelle des Herzens
Bisher gab es keine Möglichkeit zuverlässig zu untersuchen, wie hoch das Risiko eines Patienten ist, atypisches Vorhofflimmern zu entwickeln. Dank digitaler Simulationen menschlicher Organe ist es nun aber möglich, die Entstehung von Krankheiten zu erforschen und Therapien für Patienten maßzuschneidern. So haben Forscher des Karlsruher Instituts für Technologie (KIT), der Medizinischen Klinik IV des Städtischen Klinikums Karlsruhe sowie der Medizinischen Fakultät der Universität Freiburg und des Universitäts-Herzzentrums Freiburg – Bad Krozingen eine Methode entwickelt, das Risiko für Vorhofflimmern individuell abzuschätzen.

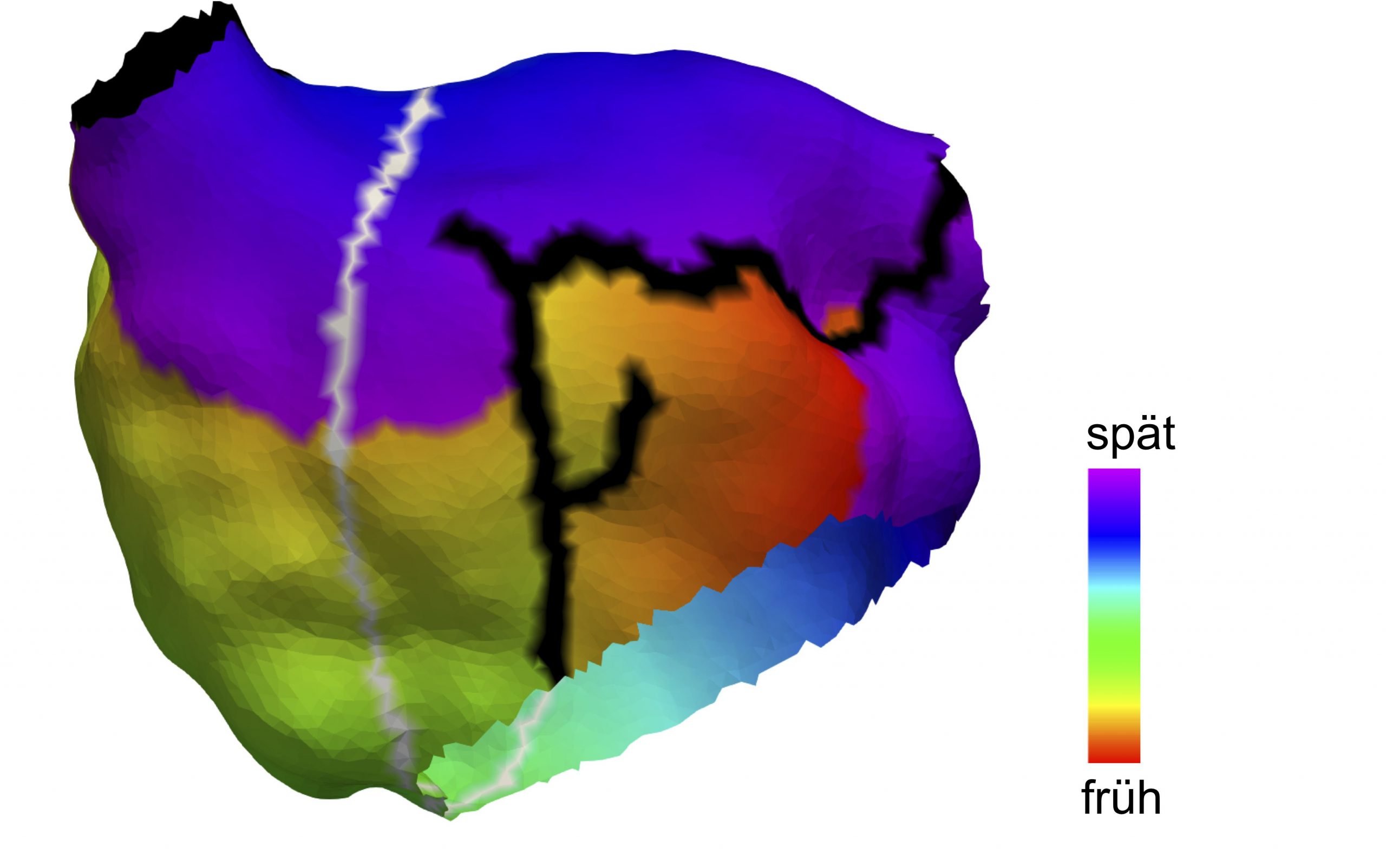
Sie entwickeln realitätsnahe Computermodelle des Herzens auf mehreren Ebenen: vom Ionenkanal über Zellen und Gewebe bis zum ganzen Organ. Dabei simulieren sie einerseits grundlegende physiologische und pathologische Prozesse und entwickeln andererseits auch personalisierte Modelle, um das Risiko von Herzrhythmusstörungen, wie z.B. Vorhofflattern, und die Wirkung von Therapien individuell abzuschätzen. In der Zeitschrift Frontiers in Physiology berichten die Wissenschaftler, dass personalisierte Computermodelle „sämtliche Pfade identifizieren können, entlang derer die atypischen, kreisende elektrischen Erregungen auftreten können.“
„Unsere Modelle beziehen anatomische, elektrophysiologische und pharmakologische Kriterien ein“, erklärt Dr. Axel Loewe, Leiter der Arbeitsgruppe Herzmodellierung am Institut für Biomedizinische Technik des KIT. Auch die Wirkung von Therapien wie Katheterablation oder Medikamenten ließe sich so vorab individuell einschätzen. „Computermodelle bieten eine perfekt kontrollierbare Umgebung für Experimente. So lassen sich einzelne Änderungen simulieren und ihre Folgen für das Gesamtsystem berechnen.“ Die Modelle würden klassische Methoden wie Zell- und Tierexperimente ergänzen und ermöglichen, neue Therapien ohne Risiko für den Menschen zu testen, betonen die Forscher.
Fachübergreifende Zusammenarbeit
Bereits in seiner Dissertation simulierte Loewe die Ursachen von Vorhofflimmern mit dem Computer und leitet nun die Arbeitsgruppe Herzmodellierung des KIT, die die neuen Computermodelle des Herzens entwickelt. An diesen Modellen können die Wissenschaftler simulieren, wie eine elektrische Erregung entsteht, sich über die Vorhöfe und das gesamte Herz ausbreitet. Bei einem gesund schlagenden Herzen erlischt diese Erregung, im Fall bestimmter Herzrhythmusstörungen bleibt sie jedoch bestehen.
Darüber hinaus arbeiten die Wissenschaftler mit personalisierten Modellen auch daran, das Risiko von Erkrankungen und die Wirkung von Behandlungen individuell zu bestimmen. Mit bildgebenden Verfahren wie der Magnetresonanztomografie (MRT) erfassen sie die die persönliche Anatomie eines Patienten, wie Größe und Form der Vorhöfe. Per Elektrokardiogramm (EKG) wird die elektrische Aktivität des Herzens aufgezeichnet. Dabei arbeiten die Wissenschaftler eng mit der ebenfalls am Institut für Biomedizinische Technik des KIT angesiedelten Arbeitsgruppe Bioelektrische Signale unter Leitung von Professor Olaf Dössel zusammen. „Die Arbeiten, die sich zwischen Ingenieurwissenschaften, Informatik, Naturwissenschaften und Medizin bewegen, bereiten den Weg zu maßgeschneiderten Therapien“, erklären die Forscher.
Titelbild: Anatomisches Modell des linken Vorhofs einer 70-jährigen Patientin. © Axel Loewe, KIT