Lange Zeit wurde es hauptsächlich als Modellsystem für die Grundlagenforschung genutzt – das Archaeon Sulfolobus acidocaldarius. Es zählt zu den extremophilen Mikroorganismen, die sich bei extrem heißen und sauren Bedingungen wohlfühlen und kann eine äußerst wertvolle natürliche Ressource sein. Dr. Julian Quehenberger, CTO beim TU Wien Spin-off NovoArc, erforschte den Mikroorganismus in seiner Dissertation bei Professor Oliver Spadiut an der TU Wien und kam so auf die Idee, diesen für industrielle Zwecke zu nutzen. 2021 gründeten Quehenberger und Spadiut gemeinsam mit Dr. David Wurm das Biotech-Unternehmen NovoArc und schafften es mit einer Spin-off Fellowship Förderung der Österreichischen Forschungsförderungsgesellschaft (FFG), die Idee zu kommerzialisieren. CEO David Wurm im Interview mit Innovation Origins:
Was ist das Problem an Spritzen?
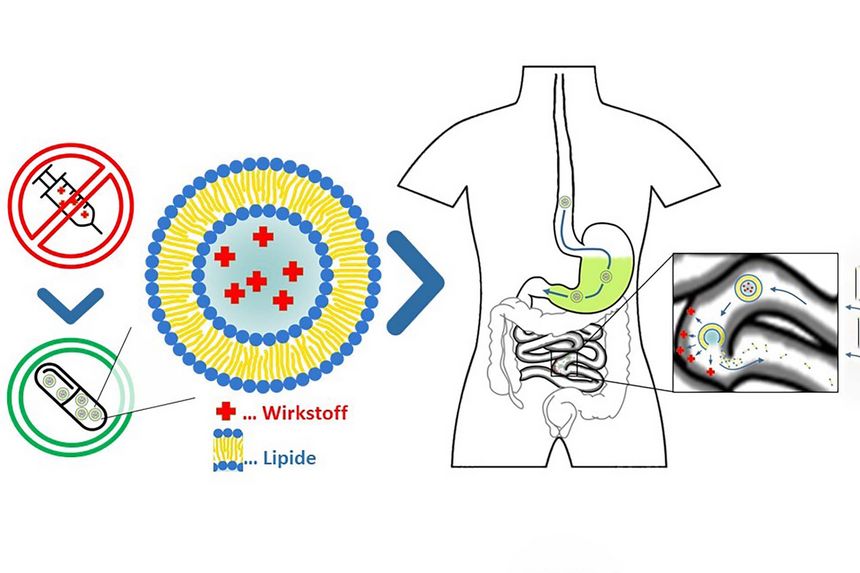
Der Grund, warum viele Wirkstoffe gespritzt werden müssen, ist deren Instabilität im Magen und die schlechte Aufnahme im Körper nach oraler Gabe. Derzeit werden chemische Beschichtungen eingesetzt, um den Wirkstoff im Magen zu schützen. Diese nehmen aber oft einen großen Teil der gesamten Tablette ein und die dabei eingesetzten Stoffe werden von den Behörden teilweise sehr kritisch gesehen. Außerdem werden Wirkstoffe mit einer schlechten Bioverfügbarkeit oft überdosiert an Patienten verabreicht, damit eine ausreichende Menge vom Körper aufgenommen wird. Das führt zu starken Nebenwirkungen, wie zum Beispiel bei Antibiotika, bei denen es zur Zerstörung der Darmflora kommen kann. Auch das aquatische Ökosystem wird dadurch stark belastet. So kommt es etwa aufgrund der ausgeschiedenen Hormone der Antibabypille zu Unfruchtbarkeit von Fischen.
Welche Lösung bietet der Mikroorganismus für dieses Problem?
Wir verwenden eine biologische Hülle aus Lipiden – sogenannte Liposome – um unterschiedliche Wirkstoffe vor Abbau im Magen zu schützen und die Aufnahme im Darm zu erhöhen. Die Lipide stammen aus der Zellmembran des extremophilen Mikroorganismus und dienen ihm als biologische Barriere gegen die harschen Umgebungsbedingungen in seinem natürlichen Lebensraum. Die Verwendung dieser Lipide wurde bereits vor einigen Jahren etabliert und in zahlreichen in vivo Studien erfolgreich für die Verabreichung von Insulin, Antibiotika, Krebstherapeutika und anderen Stoffen getestet. Der Grund, warum es noch keine Produkte mit dieser Technologie am Markt gibt, ist die Verfügbarkeit der dafür benötigten Lipide. Diese konnten bislang nicht in ausreichender Qualität und Quantität produziert werden. Uns ist es in jahrelanger Forschung gelungen, einen Produktionsprozess zu etablieren, der dieses Problem löst, wodurch die Technologie im pharmazeutischen Sektor nun endlich Anwendung finden kann.
Auch interessant: Bierhefe Saccharomyces cerevisiae Mikrobe des Jahres 2022
Wie ist diese Innovation im Forschungsumfeld einzureihen?
Es gibt derzeit unterschiedliche Ansätze, Spritzen durch Tabletten zu ersetzen, die jedoch immer auch eine Reihe von Nachteilen mit sich bringen. Dabei ist das Thema extrem wichtig. Denn mehr als 20 Prozent der gesamten Bevölkerung hat Angst vor Spritzen und viele Menschen werden beim Verabreichen von Spritzen sogar kurzzeitig ohnmächtig.
In F&E: Was war die Herausforderung?
Die größte Herausforderung war die Entwicklung eines definierten Produktionsprozesses für die benötigten Lipide. Wir stellen diese Stoffe über einen biotechnologischen Prozess mithilfe von Archaeen her. Diese Archaeen wachsen in der Natur sehr langsam und benötigen sehr komplexe Bedingungen. Sie in einer definierten und kontrollierten Laboratmosphäre reproduzierbar und skalierbar zu kultivieren, war keine einfache Aufgabe. Hier ist uns unser Know-how aus der Bioprozessentwicklung und die langjährige Erfahrung im Bereich pharmazeutischer Produktionsprozesse zugute gekommen.
Inwieweit ist das Produkt schon marktfähig?
Der pharmazeutische Markt ist sehr träge ist und darum freut es uns umso mehr, dass wir bereits einige Kooperationen mit pharmazeutischen Firmen haben und unser Produkt auch schon an diese verkauft haben. Da wir ein innovationsgetriebenes Unternehmen sind, möchten wir unser Produkt ständig weiterentwickeln. Derzeit arbeiten wir an speziellen Lipidmischungen, die wir an bestimmte Wirkstoffe anpassen. Darüber hinaus möchten wir neben dem Feld der oralen Verabreichung von Wirkstoffen auch in jenes der dermalen und nasalen Gabe von Wirkstoffen einsteigen.

Wie können wir uns Ihr Geschäftsmodell vorstellen?
Unser Kerngeschäft ist der Verkauf von Lipid-Mischungen und Lipid-Reinfraktionen sein. Bevor wir unsere Produkte an Kunden verkaufen, machen wir oft bezahlte Proof- of-Concept Studien mit pharmazeutischen Firmen, um zu zeigen, dass sich deren Wirkstoffe in unsere Liposomen verpacken lassen. Außerdem müssen die Liposomen physikochemisch, in vitro oder in vivo charakterisiert werden. Wenn diese erste Studie erfolgreich ist, wird der Prozess in einer Proof-of-Process Studie optimiert und es werden weitere Daten generiert, um besser abschätzen zu können, wieviel Wirkstoff in welcher Zeit vom Körper aufgenommen wird. Danach produzieren wir die Lipide für klinische Studien – und im letzten Schritt für den pharmazeutischen Markt. Den Enkapsulierungsschritt der Wirkstoffe transferieren wir entweder an den pharmazeutischen Partner oder führen ihn gemeinsam mit einer etablierten Formulierungsfirma durch, wie zum Beispiel Polymun, mit der wir bereits in Kontakt sind.
Inwieweit ist das Produkt umweltfreundlich?
Ein zusätzlicher großer Vorteil unserer Technologie ist die stabilisierende Wirkung unserer Lipide auf die Wirkstoffe während der Lagerung. Normalerweise müssen viele Wirkstoffe bei bis zu minus 70 Grad Celsius gelagert werden. Dies ist mit hohen Kosten, einem großen logistischen Aufwand und hohem Energieaufwand verbunden. Durch unsere Lipide soll die Lagerung von vielen Wirkstoffen bei Raumtemperatur möglich sein. Das wiederum senkt den CO2-Fußabdruck deutlich! Auch wird es somit möglich sein, Personen in abgelegenen Gebieten medizinisch zu versorgen.
Sie planen den Mikroorganismus auch für die Produktion von grünem Wasserstoff einzusetzen?
Wir wollen die stabilen Lipide von Sulfolobus auch verwenden, um neuartige Minikraftwerke für die Produktion von grünem Wasserstoff (H2) zu entwickeln. H2 ist ein kohlenstofffreier, alternativer Energieträger und wird als nachhaltiger Brennstoff der Zukunft gehandelt. Das liegt nicht zuletzt an dessen hoher gravimetrischer Energiedichte. (Anmerkung: diese beschreibt, wie viel Energie pro Gewicht (Masse) eines Rohstoffes gespeichert ist).
Der Hauptteil des heute eingesetzten H2 wird jedoch aus nicht erneuerbaren Quellen, wie Erdgas oder Kohle gewonnen. Nur ein kleiner Anteil von rund 4 Prozent wird aus Wasser durch Elektrolyse hergestellt. Nachhaltig ist die Elektrolyse aber nur, wenn der benötigte Strom aus erneuerbaren Energiequellen, wie zum Beispiel Wind oder Sonnenenergie stammt – und dass trifft erst bei 5 Prozent zu. Neuartige und nachhaltige Methoden für die Produktion von grünem H2 sind also äußerst gefragt.
Ein mögliches grünes Verfahren zur Gewinnung von Energie beziehungsweise von Wasserstoff ist die halbkünstliche Photosynthese. Bei dieser werden die für die Photosynthese zuständigen Enzyme aus Pflanzen oder Mikroorganismen in photoelektrochemischen Zellen genutzt. Diese Enzyme sind in ihrer natürlichen Umgebung in Membrane eingebettet. Wenn man sie effizient für längere Zeit nutzen will, muss man sie in eine solche Umgebung einbetten, um sie zu stabilisieren. Kürzlich wurden diese Enzyme erfolgreich in konventionelle Liposome eingebaut – dies diente jedoch einer rein grundlagenwissenschaftlichen Fragestellung. Konventionelle Lipide sind nämlich nicht stabil genug sind, um die hohen Temperaturen und dem produzierten Sauerstoff – Bedingungen bei der Photosynthese – standzuhalten.
Wir wollen grünen H2 nachhaltig aus Licht und Wasser in stabilen Minikraftwerken produzieren. Dazu werden wir die photoaktiven Bausteine in CO2-negativen Prozessen biotechnologisch gewinnen und in NovoArcs stabile Lipide verpacken. Einen entsprechenden FFG Projekt-Antrag werden wir in 2022 einreichen.
Auch interessant: Hefen als alternative Eiweißquelle für Tierfutter


