Het 3D-bio-printlaboratorium van de Medische Universiteit van Innsbruck werkt aan de productie van menselijk weefsel dat met 3D-bioprinters kan worden opgebouwd. Dit kunstmatig gefabriceerde model van menselijk weefsel maakt het mogelijk ziekten te simuleren en te bestuderen. Onlangs is het onderzoeksteam erin geslaagd een 3D-model voor de tumormicro-omgeving te ontwikkelen. Daarmee kan de ontwikkeling van tumoren en de doeltreffendheid van kankermedicijnen in real time worden bestudeerd.
Het 3D-model voor de tumormicro-omgeving is een combinatie van complex vaatweefsel en een vloeistofchip. De chip meet 28 bij 21 millimeter. Het werkt volgens de principes van de microfluïdica, die zich bezighoudt met het gedrag van vloeistoffen en gassen in een zeer kleine ruimte. Dit kan aanzienlijk verschillen van het gedrag van macroscopische vloeistoffen, omdat op deze schaal effecten kunnen overheersen die in de klassieke vloeistofmechanica vaak worden verwaarloosd.
Groeiend weefsel
Dergelijke microfluïdische apparatuur wordt reeds gebruikt op het gebied van de celkweek, maar heeft meestal slechts één cellaag. Het weefsel uit Innsbruck wordt echter tot een dikte van drie millimeter geprint. En net als in het menselijk lichaam ontwikkelt zich daarin een dicht driedimensionaal capillair netwerk.
Dit nagebootste menselijk weefsel is gebaseerd op een driedimensionale hydro-gel, die laag voor laag met cellen wordt opgebouwd in de 3D-bioprinter. Voor het nieuw ontwikkelde 3D-model van de tumormicro-omgeving wordt het nagebouwde menselijke weefsel rechtstreeks in de fluïde chip van plexiglas geprint, waar het vervolgens op natuurlijke wijze en uit zichzelf groeit.
Hierdoor worden bijna-reële omstandigheden gecreëerd, die het mogelijk maken in real time en in detail te onderzoeken hoe de tumor zijn omgeving manipuleert en in zijn eigen voordeel gebruikt. Het van menselijk weefsel afgeleide equivalent kan op een gestandaardiseerde manier worden geproduceerd. Het kan daardoor dierproeven vervangen. Voor het 3D-model is octrooi aangevraagd.

Verbinding tussen chip en weefsel
Vóór het afdrukken worden fijne kanalen in het plexiglas gelaserd, zodat de fijne kanalen in het complexe vaatweefsel rechtstreeks op de chip kunnen worden aangesloten. Het weefsel heeft dan drie weken nodig om te groeien en te rijpen. De cellen binnenin gebruiken deze tijd om zich te organiseren. Hierdoor verandert ook het volume van het weefsel en kan het loskomen van het plastic.
Om dit te voorkomen, hebben de onderzoekers de chip zo ontwikkeld dat het weefsel ermee verbonden blijft. Hierdoor kan het levende weefsel wekenlang stabiel en verankerd blijven, aldus laboratoriumhoofd en microbioloog Michael Außerlechner. De onderzoekers zijn er ook in geslaagd met de bio-printer fijne haarvaten te genereren die lijken op bloedvaten, zodat alle cellen in het weefselmodel voldoende kunnen worden bevoorraad. De bloedvaten hebben een diameter van ongeveer 0,3 millimeter en vormen de voornaamste toevoerwegen in het weefselmodel.
Haarvaten
Bovendien zijn er fijne haarvaten nodig om cellen in het weefsel te bevoorraden die verder van deze kanalen verwijderd zijn. Ook hiervoor hebben de onderzoekers een oplossing gevonden. Zij ontwikkelden een speciale bio-inkt waarmee ze endotheelcellen in de chip printen. Deze bekleden de binnenkant van de bloedvaten. Zij vormen in het model een fijn capillair netwerk en doordringen binnen zes tot zeven dagen het hele weefsel”, zegt biotechnologe Judith Hagenbuchner, die samen met Außerlechner aan het hoofd staat van het 3D-bio-printing lab.
Wondgenezing
Het aldus in gang gezette proces is vergelijkbaar met de natuurlijke wondgenezing. Het model kan voor vele vragen worden gebruikt. Het maakt bijvoorbeeld het testen van zogenaamde angiogeneseremmers mogelijk. Angiogenese verwijst naar de vorming van nieuwe bloedvaten. Angioneseremmers hebben tot taak de vorming van nieuwe bloedvaten en dus de groei van tumoren te onderdrukken. Met het 3D-model voor de micro-omgeving van tumoren kan zo een op de patiënt toegesneden therapie worden ontworpen. Volgens de onderzoekers is het weefselmodel dus ook een belangrijke stap in de richting van precisiegeneeskunde. Het nieuw ontwikkelde platform zou zelfs geschikt kunnen zijn voor onderzoek naar metastase – een proces dat de kans op genezing bij kanker aanzienlijk verslechtert.
Tumoren bij jonge kinderen
Außerlechner leidt ook het laboratorium voor moleculaire biologie van de afdeling kindergeneeskunde. Het lag dus voor de hand om een neuroblastoom te onderzoeken. Dit is een van de meest voorkomende tumoren bij jonge kinderen, die nog steeds een slechte prognose heeft. Het doel van het project is therapieën te ontwikkelen tegen de groei en uitzaaiing van de tumor. Met het nieuwe 3D-model kunnen de onderzoekers de omgeving van de tumor nabootsen en de reactie van de tumor op het geneesmiddel op een patiënt-specifieke basis vaststellen.
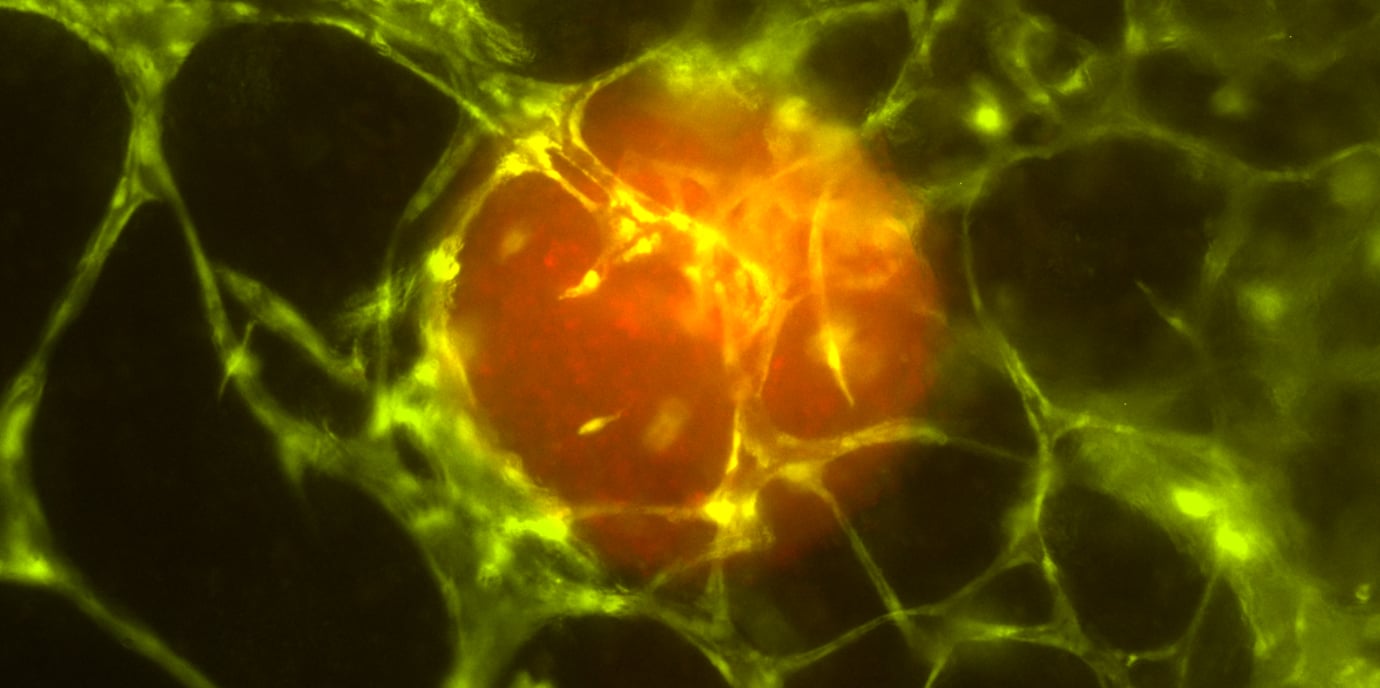
In het experiment werden de bolvormige tumorcelaggregaten, zogenaamde tumorsferoïden, van een neuroblastoom tijdens het printproces tussen de cellen van het 3D-geprinte weefsel geplaatst. Daar groeiden ze binnen twee tot drie weken uit tot een microtumor. De onderzoekers konden waarnemen hoe deze kleine tumor de haarvaten uit het weefsel aantrekt en hoe deze vervolgens uitgroeien tot de tumor. Dit laat zien hoe de tumor actief zijn eigen voorraadstructuur opbouwt.
Op basis van de eerste resultaten moeten specifiek op patiënten afgestemde therapieën en testsystemen worden ontwikkeld. Het 3D-model zal helpen om de mechanismen van een tumorgroei nog beter te begrijpen en zo de tumormicro-omgeving bruikbaarder te maken als therapeutisch doelwit voor kankerbestrijding. En zonder dierproeven”, benadrukt Außerlechner.
Het onderzoek werd onlangs gepubliceerd in het vakblad Biofabrication.

