Als je ziek bent, ben je blij dat je een medicijn krijgt. Als echter de werkzame stof ook in gezonde cellen terecht komt, kan dat tot nare bijwerkingen leiden. Denk maar aan chemotherapie, waarvan de bijwerkingen meestal compleet haarverlies zijn.
Een onderzoeksteam onder leiding van Prof. Oliver Lieleg, hoogleraar biomechanica aan de Munich School of BioEngineering van de TUM, en Prof. Thomas Crouzier van de Koninklijke Technische Hogeschool (KTH) in Stockholm hebben nu een stabiele nanoverpakking voor geneesmiddelen ontwikkeld, waardoor de werkzame stof alleen binnen de aangetaste cellen vrijkomt.
Eiwitruggengraat
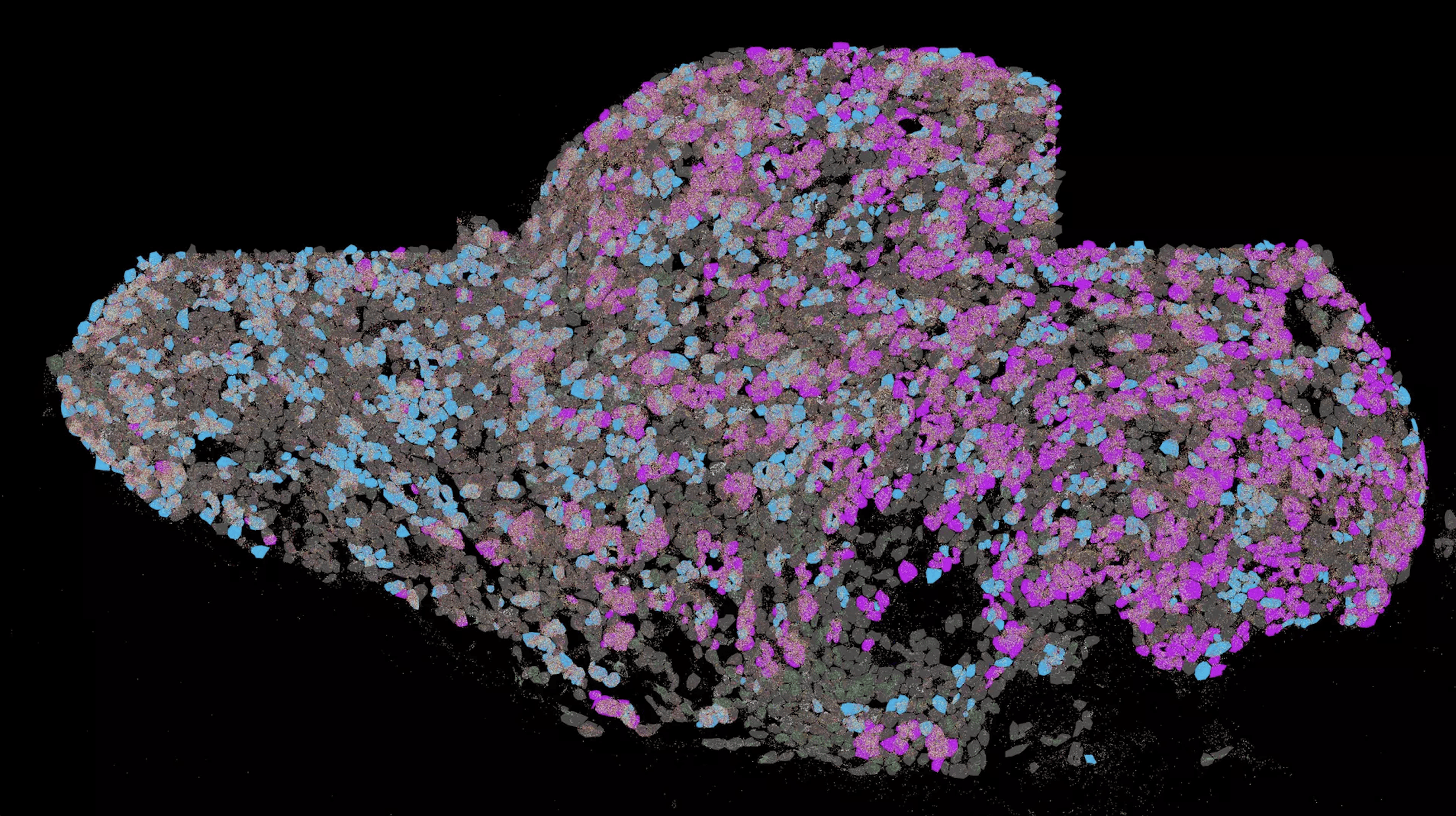
In een studie in tumormodelsystemen uit celculturen heeft dit mechanisme al gewerkt. De wetenschappers hebben de werkzame stoffen eerst verpakt met behulp van zogenaamde mucines, die bestaan uit een eiwitruggengraat waaraan suikermoleculen zijn vastgehecht. Slijmstoffen zijn belangrijke bestanddelen van het slijm dat in de mond, de maag of de darmen wordt geproduceerd. “Aangezien slijmstoffen in het lichaam voorkomen, kunnen geopende slijmdeeltjes later door de cellen worden afgebroken,” zei Lieleg.
Een ander belangrijk bestanddeel van mucines wordt ook in het lichaam gevonden: desoxyribonucleïnezuur (DNA). Het draagt onze genetische informatie. De onderzoekers synthetiseerden DNA-structuren met de gewenste eigenschappen en bevestigden deze chemisch aan de mucines: “Als er glycerol wordt toegevoegd aan de oplossing die de mucine-DNA-moleculen en het actieve ingrediënt bevat, neemt de oplosbaarheid van de mucines af, ze vouwen zich op en sluiten het actieve ingrediënt in”, leggen de wetenschappers uit. “De DNA-strengen binden zich aan elkaar en stabiliseren de structuur, zodat deze zich niet meer vanzelf kan ontvouwen.”
Slot en sleutel
Alleen de juiste “sleutel” kan de DNA-gestabiliseerde deeltjes weer openen. Pas dan kunnen de ingekapselde medicijnmoleculen vrijkomen. Zogenaamde microRNA-moleculen dienden als sleutel, aangezien RNA (ribonucleïnezuur) qua structuur sterk lijkt op DNA en een belangrijke rol speelt bij de eiwitsynthese in het lichaam. Het kan echter ook andere celprocessen reguleren.
“Kankercellen bevatten microRNA-strengen waarvan we de structuur precies kennen,” verklaart Ceren Kimna, eerste auteur van de studie. “Om ze als sleutel te gebruiken, hebben we het slot dienovereenkomstig aangepast – door zorgvuldig de synthetische DNA-strengen te ontwerpen die onze drugsdragende deeltjes stabiliseren. De DNA-strengen zijn zo ontworpen dat de microRNA-moleculen zich eraan kunnen binden, waardoor de bestaande bindingen die de structuur stabiliseren, worden verbroken. De synthetische DNA-strengen in de deeltjes kunnen ook worden aangepast aan microRNA-structuren die voorkomen bij andere ziekten zoals diabetes of hepatitis.”
verder onderzoek nodig
Het zal echter nog enige tijd duren voordat deze nieuwe methode op patiënten kan worden toegepast. De onderzoekers benadrukken dat verder onderzoek in het laboratorium met complexere tumormodelsystemen nodig is voordat dit kan gebeuren. Daarnaast zijn ze ook van plan om “verdere wijzigingen van dit medicijnverlichtingsmechanisme te onderzoeken om de bestaande kankertherapieën te verbeteren”.