Wetenschappers zijn weer een stap dichterbij het antwoord gekomen op de vraag hoe de ziekte van Alzheimer ontstaat. Het gaat daarbij over veranderingen van eiwitstructuren in het brein. Het is onderzoekers van de Universiteit Ulm voor de eerste keer gelukt deze eitwitvezels (beta amyloïde fibrillen) uit hersenweefsel van Alzheimerpatiënten te isoleren en te onderzoeken. Er moet nog wel veel verder onderzoek volgen.
Bij mensen die lijden aan de ziekte van Alzheimer, sterven de zenuwcellen in de hersenen en de verbindingen tussen deze cellen geleidelijk aan af. Wereldwijd lijden bijna 47 miljoen mensen aan deze meest voorkomende vorm van dementie. De oorzaak van deze ziekte is nog steeds een mysterie voor onderzoekers. Wetenschappers gaan er tot nu toe vanuit dat eiwitvezels -de zogenaamde neuro-fibrilbundels- die niet goed door de hersenen worden afgebroken, de ziekte veroorzaken. Deze afzettingen zijn altijd aantoonbaar in de hersenen van Alzheimerpatiënten.
De Alzheimer-onderzoekers zien met name twee eiwitten, tau en bèta-amyloïde, als bijzonder pathogeen (biologische ziekteverwekker). Deze eiwitten hopen zich op in vezelklonten in de hersenen die zich hebben gevormd uit moleculaire ketens; fibrillen. De vraag, waarom de lichaamseigen eiwitten zich abnormaal ontwikkelen en vervolgens leiden tot veranderingen in de hersenen, is nog niet opgehelderd.
Grote verschillen met kunstmatig geproduceerd onderzoeksmateriaal
De onderzoekers ontdekten dat de vezels aanzienlijk verschillen van de synthetisch geproduceerde vezels die in het onderzoek worden gebruikt. De afzonderlijke peptiden waaruit de fibrillen bestaan, verschilden van die welke kunstmatig in de reageerbuis werden geproduceerd.
Ten tweede vertoonden de structuren een heel andere manier draaiing dan bij synthetische fibrillen. “Dit is een fundamenteel andere eigenschap, die we niet hadden verwacht”, aldus professor Marcus Fändrich, hoofd van het Instituut voor Eiwitbiochemie aan de Universiteit van Ulm. In hun studie onderzochten de onderzoekers de weefselmonsters van drie patiënten. Ze vonden bij alle drie de patiënten dezelfde structuren.

De wetenschappers uit Ulm, Tübingen, Halle an der Saale en San Diego hebben meer dan vier jaar intensief wetenschappelijk onderzoek verricht werk voordat ze tot deze conclusie konden komen. De grootste uitdaging was het verwijderen van de bèta-amyloïde fibrillen uit de weefselmonsters en deze in verschillende stappen te zuiveren. Bovendien vertoonden de fibrillen onder de cryo-elektronenmicroscoop talrijke verschillende subtypes, wat de analyse nog moeilijker maakte.
Meer artikelen over Alzheimer kunt u hier vinden.
De onderzoekers leggen uit dat deze bevindingen hen een stap dichter bij het ontcijferen van de oorzaken van Alzheimer kunnen hebben gebracht. Er is namelijk nu veel meer bekend over de structuren die bèta-amyloïde in de hersenen aanneemt en zo de ziekte kan veroorzaken. “Wetenschappers moeten nu in het laboratorium de omstandigheden vinden die tot de vorming van deze structuren leiden”, benadrukt Fändrich. Er kan voorts verder onderzoek plaatsvinden op basis van deze bèta-amyloïde structuren. Het moet nog blijken of de gevonden inzichten over de bèta-amyloïdestructuur gebruikt kunnen worden voor de ontwikkeling van farmaceutisch werkzame stoffen”.
De studie is gepubliceerd in het tijdschrift Nature Communications.
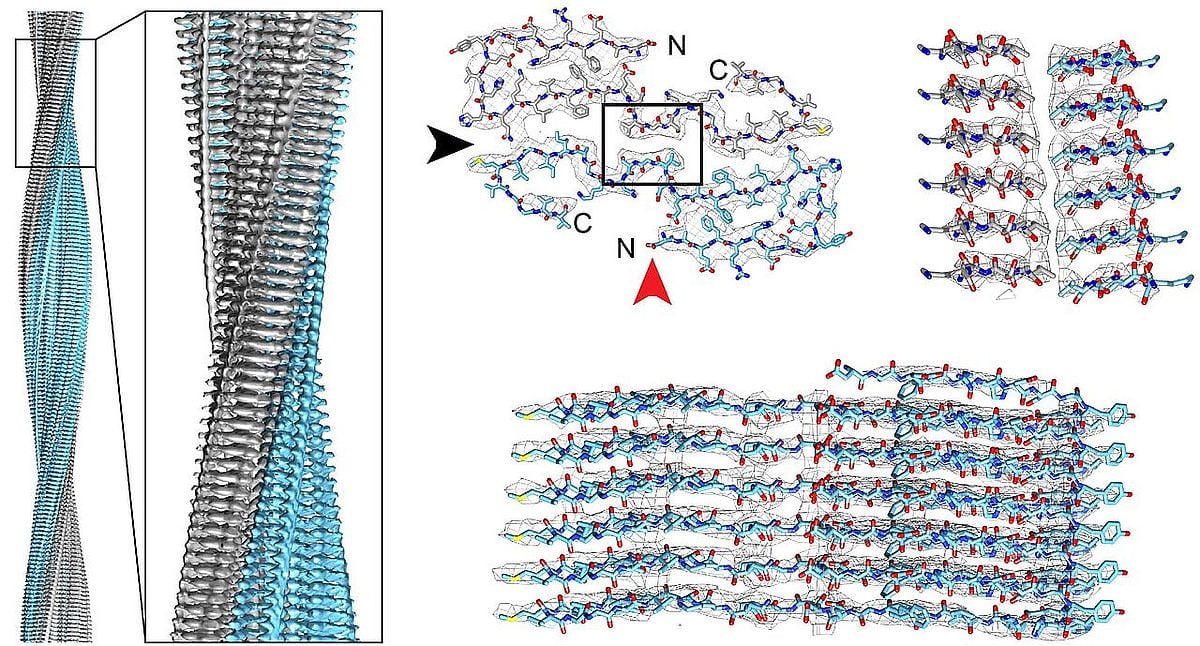
Titelfoto: Zijaanzicht van een aß-amyloïde fibril (links), doorsnede van een fibrillair vlak (midden bovenin). Het gehele fibril bestaat uit meerdere gestapelde lagen (rechtsonder); © Kollmer et al., Nature Communications