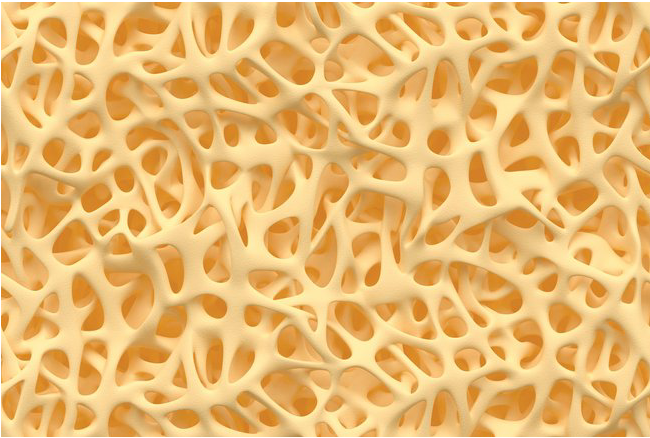
Onderzoekers van de Technische Universiteit Eindhoven (TU/e) en Radboudumc zijn erin geslaagd uit menselijke stamcellen een levensecht stukje botweefsel laten groeien. Het gaat hierbij om de eerste ‘organoïde’ van bot, een versimpelde versie van het origineel. Het onderzoek is deze week gepubliceerd in het blad Advanced Functional Materials. Het gekweekte bot bijzonder geschikt voor het testen en ontwerpen van nieuwe behandelingen voor botaandoeningen als osteoporose of osteogenesis imperfecta.
De wetenschappers verweefden diverse botcellen met elkaar tot een zogenoemd ‘organoïde’. Dit mini-orgaantje kan zelfstandig nieuw, hard botweefsel maken. In de toekomst wordt het daardoor mogelijk om behandelingen heel nauwkeurig op de patiënt af te stemmen.
Met stamcellen afkomstig uit het beenmerg van een patiënt kan in een laboratorium een stukje botweefsel worden gekweekt. Vervolgens kijken artsen welke medicijnen op die botten het gewenste effect hebben. Op die manier zou voor iedereen een behandelplan op maat gemaakt worden.

Bij botvorming spelen drie soorten cellen de hoofdrol: osteoblasten (die botweefsel opbouwen), osteoclasten (die bot afbreken) en osteocyten (die de opbouw en afbraak van bot reguleren). “De meeste onderzoeken tot nu toe richtten zich op één van deze typen cellen. Maar dat is geen goede weergave van echt weefsel”, zegt Hofmann. “We presenteren hier een stukje gegroeid bot dat twee van deze typen cellen bevat: osteoblasten en osteocyten. We zien nu dat we uitsluitend met deze twee celtypen levensecht bot kunnen maken.”
Versimpelde weergave
Dat er nu een versimpelde weergave mogelijk is van de vorming van bot op moleculair niveau, biedt volgens de onderzoekers ongekende mogelijkheden. “Een bot bestaat voor 99 procent uit collageen en mineralen, en de rest is eiwit”, legt professor Nico Sommerdijk van Radboudumc uit. “Wat is de rol van die eiwitten? Hoe ondersteunen ze de botvorming? Nooit eerder konden we op moleculair niveau de mijlpalen van dit proces bekijken.”
Daarmee hebben ze direct een goede ingang om van pijnlijke botproblemen als ‘broze botten ziekte’ en de mogelijke behandelingen te onderzoeken. “Bedenk dat de oorsprong van veel aandoeningen op moleculair niveau zit – en de behandeling dus ook”, zegt Akiva. “Feitelijk hebben we nu een simpel systeem in een betrouwbare omgeving waarin we kunnen porren en kijken hoe de botcellen reageren op de stimuli die we geven.”
Lees hier de oorspronkelijke publicatie.
Ook interessant: “Iets kapot in je lichaam? Dan maakt de dokter straks een nieuw orgaan of bot.